Desalinizzatori- demineralizzatori verticali a scambio ionico con produzione di energia idroelettrica.
Desalinizzatori- demineralizzatori verticali a scambio ionico con produzione di energia idroelettrica.
Deposito di brevetto italiano N. 102016000057968 del 07/06/2016
Riassunto
Lo stato dell’arte nello sviluppo dei trattamenti di desalinizzazione e demineralizzazione delle acque marine e salmastre è stato condizionato, come molti altri sistemi industriali, depurativi, energetici e protettivi dell’ambiente, dall’assenza di sinergie tra le pompe e le turbine idrauliche e dall’errato approccio con la forza gravitazionale, che non deve essere vinta dai sollevamenti idraulici ma assecondata, con circolazione d’acqua a senso unico in serbatoi aperti, posti in alto che fungono anche da disconnettori idraulici. Con la tripla sinergia tra le pompe a doppia alimentazione, le turbine e il riciclo dell’acqua in vaso aperto, applicando principi idraulici noti da secoli, come il principio dei vasi comunicanti, le leggi di Bernoulli e Pascal, ponendo strategicamente le elettropompe a doppia aspirazione tra un alto battente idraulico positivo e le turbine, possiamo dissalare grandi quantità di acqua, semplicemente trasformando un tubo verticale in uno scambiatore ionico e i tubi di riciclo e miscelazione in produttori di energia, mentre le resine sintetiche anioniche e cationiche, circolano contenute in sfere di polietilene forate come setacci. Tali sfere, galleggiano risalendo lo scambiatore ionico e discendono per gravità svuotandosi dell’acqua nei tubi di discesa. Per mezzo di deviatori cambiano il percorso rispetto al flusso dell’acqua per essere immerse in vasche di lavaggio e rigenerazione delle resine, e reinserite di nuovo, all’infinito, nel circuito di scambio ionico senza interruzione del ciclo di dissalazione e della produzione energetica e senza costi per riscaldare l’acqua o sostituire le membrane. L’acqua demineralizzata che serve per il lavaggio delle resine è prodotta proseguendo il processo attraverso un mini impianto del tutto simile a quello principale che parte dal serbatoio delle acque dissalate. Se gli uomini vogliono produrre acque dissalate nelle quantità industriali che servono all’umanità, anche i desalinizzatori devono diventare impianti globali, produttori, non consumatori di energia, insieme ai depuratori ai sollevamenti e alla distribuzione idrica, assecondando, non contrastando le forze gravitazionali. La sostenibilità degli impianti globali non si basa su tecnologie complicate ma sulle sinergie tra impianti semplici e razionali
DESCRIZIONE
Allo stato attuale della tecnica di dissalazione e demineralizzazione fanno capo tre tipologie di impianti: per evaporazione, permeazione per mezzo di membrane, per scambio ionico. Attualmente, la differenza tra i tre sistemi, sopra citati, la fa soprattutto il costo del trattamento.
Quella evaporativa, produce acque prive di sali minerali e con PH acido, quindi per l’utilizzo dell’acqua è necessaria una successiva mineralizzazione e la neutralizzazione del PH.
La filtrazione con membrane comporta alte pressioni di esercizio, quindi alti consumi energetici e l’alto costo delle membrane, che periodicamente devono essere sostituite.
Quella con le resine di scambio ionico comportano un complesso circuito di filtrazione lavaggio rigenerazione delle resine, con flussi inversi che comportano la dispersione di una parte delle resine nelle acque di scarico dei processi.
Tutti i processi comportano alti consumi energetici per il riscaldamento oppure per la circolazione in pressione delle acque nei sistemi di filtrazione e rigenerazione. I costi di esercizio si aggirano intorno a 1,5 euro/mc con gli impianti a osmosi inversa, che sono quelli più usati, ma anche i costi di investimento sono notevoli, essendo di circa 1000 euro per ogni m3/giorno di acqua dissalata prodotta. E’ ovvio che con questi costi di produzione e di investimento, l’acqua dissalata può essere utilizzata solo per uso potabile. E’ impossibile pensare di impiegarla per l’industria e l’agricoltura. Con la soluzione che si propone l’impiego agricolo e industriale diventerà una realtà competitiva anche con i pozzi e gli altri sistemi depurativi, che comunque sono costretti a trattare acque inquinate, o con scarsi requisiti minerali. Infatti, l’acqua marina essendo ricchissima di sali minerali, se la desalinizzazione diventa sostenibile, può diventare il migliore concime naturale dei terreni, potendo inviare agli stessi un’acqua utilizzabile anche come concime trattata su misura per il terreno di destinazione, sia in termini di Sali minerali che di alcalinità. Per il trasporto dell’acqua dissalata a notevoli distanza non c’è nessun problema perché con le pompe a doppia alimentazione abbinate alle turbine idrauliche, anche il trasporto e il sollevamento delle acque diventa una fonte energetica, non di consumo. Infatti, la chiave per risolvere molti problemi ambientali ed energetici, compresa la dissalazione, è quella di realizzare circuiti idraulici e idroelettrici che utilizzano diversamente le pompe e le turbine.
Allo stato dell’arte il sistema di dissalazione meno impiegato è quello con lo scambio ionico, ma questo sistema è il più adatto ad essere utilizzato in abbinamento con le pompe a doppia alimentazione e le turbine, non avendo la necessità di alte temperature o di altre pressioni di esercizio rispetto ai sistemi concorrenti. Pertanto, l’alto costo delle resine e dei liquidi reagenti, necessari per la rigenerazione, potrà essere ampiamente compensato dal basso consumo energetico, dalla produzione energetica prodotta dall’impianto, dal basso costo dell’impiantistica necessaria, e dai bassi costi di gestione e manutenzione. Inoltre, con la soluzione di seguito descritta, sarà risolto anche il problema della dispersione delle resine nelle acque e nei liquidi di processo, essendo le resine contenute e fatte circolare (nell’acqua e nei reagenti chimici) in sfere di polietilene forate con fori di passaggio inferiori alla dimensione delle stesse. Si può dire, che la nuova soluzione è opposta alle attuali soluzioni di scambio ionico, dove le resine sono ferme e il liquido le attraversa, sia nelle fasi di reazione che in quelle di lavaggio e rigenerazione. Con il sistema proposto le resine le resine circolano nell’acqua e nei liquidi rigeneranti, a bassa velocità, con lunghi tempi di contatto, che assicurano contatti capillari. Per la circolazione si sfruttano principi fisici, non energetici. Oltre il 90% dell’energia prodotta nell’impianto può essere trasferito alle reti elettriche pubbliche.
Quindi l’impianto è composto da una parte chimica, una elettromeccanica e una idraulica.
La chimica dello scambio ionico.
Dalla letteratura scientifica, si può apprendere che lo scambio ionico, è un processo in cui ioni di una data specie sono sostituiti sulla superficie di un materiale non solubile di scambio (resina a scambio ionico) da ioni di una specie differente disciolti in soluzione. Si compone di due fasi: cationica e anionica. Nell’impianto proposto, che si sviluppa in verticale, tali fasi avverranno separatamente in tubi di grande diametro (5) facendovi transitare a bassa velocità una adeguata quantità di sfere in polietilene a bassa densità forate come un setaccio, contenenti granuli di resine anioniche o cationiche selezionate con diametro superiore a fori di passaggio, in quantità proporzionali ai sali da assorbire. Le resine a scambio ionico possono essere sia naturali che sintetiche.
Le resine naturali sono le zeoliti (allumino-silicati) utilizzate soprattutto per l’addolcimento delle acque e per la rimozione dello ione ammonio.
Le resine sintetiche sono formate da polimeri fenolici che si presentano generalmente sotto forma di piccole sfere di diametro compreso fra 0,3 e 1,3 mm. Con una densità di 1,2-1,3 Kg/l. Possono essere di due tipi:
a) a struttura gelulare: traslucide, scarsa elasticità, capacità più elevata;
b) a struttura macroporosa: opache, elevata porosità, minore capacità;
la struttura di base dei due tipi è comunque identica essendo entrambe ottenute per copolimerizzazione. La realizzazione delle resine sintetiche avviene generalmente tramite un processo di copolimerizzazione fra stirene e divinilbenzene. Lo stirene ha funzione di matrice della resina, mentre il divinilbenzene serve per dare consistenza alla resina. Le proprietà principali delle resine scambiatrici sono:
– la capacità di scambio: viene espressa in eq/L o eq/Kg. Essa viene definita come la quantità di uno ione di scambio che la resina può portare.
– la dimensione delle sfere di resina: l’importanza della dimensione risiede nel fatto che la cinetica, nonché il tasso di scambio ionico nelle colonne è funzione della stessa. In generale il tasso di scambio ionico è inversamente proporzionale al quadrato del diametro delle particelle.
La capacità di scambio dichiarata di una resina varia in base al tipo ed alla concentrazione di sostanza utilizzata per rigenerare la resina. Generalmente la capacità di scambio di una resina sintetica varia fra 2 e 10 eq/Kg resina, mentre le zeoliti cationiche hanno una capacità di scambio compresa 0.05 e 0.1 eq/Kg resina.
Spesso la capacità di scambio delle resine viene espressa in termini di grammi di CaCO3 per m3 di resina (g/m3) o grammi equivalenti per m3 (g eq/m3).
Il livello rigenerativo: è la quantità di rigenerante (HCl, H2SO4, NaOH) considerato al 100% necessario per rigenerare un litro di resina. Si esprime in grammi di rigenerante per litro di resina.
La capacità di scambio totale: E’ la concentrazione di siti attivi per unità di misura. E’ riferita all’unità di volume (Eq/litro) o di peso (Eq/grammo) ed è un parametro indicato nelle schede tecniche delle resine.
La capacità operativa di scambio: è la quantità di ioni (Eq/litro o g CaCO3/litro) che una determinata resina scambia nelle specifiche condizioni di esercizio in cui è utilizzata.
Gli schemi di processo variano in funzione dell’obiettivo del trattamento da effettuare.
Alcuni trattamenti classici realizzabili con le resine di scambio ionico sono: Addolcimento, decarbonatazione (demineralizzazione parziale) demineralizzazione completa, rimozione di specifichi metalli pesanti, ma sostanzialmente, lo scambio ionico, come l’ultra filtrazione, se diventa sostenibile ed energetico è anche un ottimo sistema depurativo terziario. Soprattutto, se considera che consente di avere l’uscita delle acque già sollevate, che possono essere distribuite senza costi aggiuntivi.
Come detto inizialmente lo scambio ionico in generale comporta lo scambio di uno ione presente sul gruppo funzionale della resina con uno ione di pari carica presente in soluzione. Fra questi un caso particolare riguarda le cosiddette resine cationiche in ciclo sodico, del tipo cioè R-Na, ove al posto dell’idrogenione delle resine cationiche in ciclo acido, troviamo lo ione Na+. Tali resine pertanto durante la fase di esaurimento non scambieranno ione H+, bensì rilasceranno lo ione Na+ al posto di quello che prendono. Queste particolari resine vengono di solito ottenute salificando le resine cationiche acide del tipo R-SO3H andando a sostituire lo ione H+ con lo ione Na+ e sono utilizzate per rimuovere la durezza delle acque in quanto lo ione Na+ ha particolare affinità di scambio con gli ioni Ca++ e Mg++ secondo le reazioni sopra citate. La rigenerazione delle resine cationiche in ciclo sodico avviene tramite un lavaggio in salamoia (soluzione al 10% di NaCl). L’addolcimento prevede perciò l’uso di una resina cationica forte in ciclo sodico, come visto lo scambio avviene fra gli ioni Ca++ e Mg++ in soluzione e lo ione Na+ sulla resina. Può essere considerata una demineralizzazione parziale, limitata alla rimozione degli ioni di Ca++ e Mg++. Un tipico esempio di addolcimento può avvenire usando resine cationiche in ciclo sodico tramite reazioni del tipo: CaSO4 + Na+ ↔ NaSO4 +Ca++ Si ottiene così in soluzione del solfato di sodio solubile al posto del solfato di calcio che è quasi insolubile. Tramite rigenerazione con soluzione di NaCl si ottiene la rigenerazione della resina la quale si ricarica di ioni Na+ e rilascia gli ioni Ca++ che si legano al cloruro Cl- dando cloruro di calcio CaCl2 relativamente inerte. L’addolcimento a differenza della demineralizzazione non rimuove i solidi disciolti, bensì li modifica chimicamente.
La decarbonatazione è anch’essa una demineralizzazione parziale in cui si utilizza una resina cationica debole seguita da uno strippaggio dell’anidride carbonica formatasi tramite una torre di degasaggio. Con la resina cationica debole vengono scambiati solo i cationi legati ai bicarbonato. L’acidità che si genera nell’acqua a causa del rilascio di idrogenioni da parte della resina e la presenza dello ione HCO3-, porta allo spostamento dell’equilibrio carbonatico verso la produzione di acido carbonico H2CO3 e quindi di CO2 libera secondo la reazione:
R-COOH + HCO3X ↔ R-COOX + H + + HCO3-; HCO3- +H+↔ H2CO3 ↔ H2O + CO2↑
Lo strippaggio della CO2 consente lo spostamento a dx della reazione e l’eliminazione del H2CO3. Questo processo permette la rimozione dei sali legati ai bicarbonati, da cui il nome di decarbonatazione o demineralizzazione parziale.
Allo stato dell’arte si distinguono cinque tipi di resine sintetiche a scambio ionico:
1) Resine cationiche forti, 2) Resine cationiche deboli, 3) Resine anioniche forti, 4) Resine anioniche deboli, 5) Resine selettive chelanti per metalli pesanti.
– Le resine cationiche forti si comportano in maniera simile ad un acido forte e vengono fortemente ionizzate sia nella loro forma acida (R-SO3H) che in quella salina (RSO3Na) in un ampio spettro di valori di pH.
– Le resine cationiche deboli hanno un gruppo funzionale acido debole, tipicamente un gruppo carbossilico (COOH). Queste resine si comportano come acidi deboli e come tali hanno un basso grado di dissociazione.
– Le resine anioniche forti vengono fortemente ionizzate grazie a gruppi basici forti quali l’anione idrossile (OH) e possono essere utilizzate in tutto il campo di pH. Grazie al gruppo idrossile OH sono spesso utilizzate per la deionizzazione dell’acqua.
– Le resine anioniche deboli sono portatrici di gruppi basici deboli e pertanto hanno un grado di ionizzazione dipendente dal pH, generalmente ionizzano in campi di pH ristretti.
Le resine chelanti selettive per metalli pesanti si comportano come resine cationiche forti, presentando però un alto grado di selezione nella capacità di chelare i cationi di metalli pesanti.
Tipicamente, le resine cationiche scambiano un idrogenione H+ presente sul gruppo funzionale con i cationi presenti in soluzione ( Na+, K+, Ca++, Mg++, Cu++, Ni++, Pb++, Zn++, Fe++, etc.). Alla fine della reazione l’acqua risulterà impoverita dei propri cationi e ricca di ioni idrogeno (pertanto acida).
Tipici gruppi funzionali che si trovano sulle resine a scambio cationico ed in grado di scambiare idrogenioni, sono:
Gruppo solfonico: R-SO3H, il quale essendo il radicale di un acido forte scambia con tutti i cationi presenti in acqua in un vasto campo di pH, da cui l’appellativo conseguente di resine cationiche forti.
Gruppo carbossilico: R-COOH, il quale essendo il radicale di un acido debole risulta dotato di una forte affinità solo nei confronti di cationi legati a bicarbonato, da cui l’appellativo di resine cationiche deboli Es.: R-H + Na+ ↔ R-Na + H+.
Viceversa le resine anioniche scambiano tipicamente ossidrilioni, cioè ioni OH- presenti sui loro gruppi funzionali con gli ioni presenti in soluzione (Cl-, SO42-, HCO3-, CN–, etc.). Tipici gruppi funzionali in grado di rilasciare ossidrilioni e prendersi gli ioni presenti in acqua, sono:
Gruppo ammonico quaternario: R-N(CH3)3OH il quale essendo il radicale di una base forte scambia con tutti i tipi di anioni, da cui il nome di resine anioniche forti.
Gruppo amminico: R-NH3OH il quale essendo il radicale di una base debole è dotato di una forte affinità di scambio solo con gli anioni di acidi forti, tipicamente Cl– e SO42-, da cui il nome di resine anioniche deboli. Es: R-OH + Cl– ↔ R-Cl + OH–.
Si noti che le reazioni di scambio ionico sono delle vere e proprie reazioni chimiche di equilibrio e come tali reversibili. A tal proposito il ciclo lavorativo di una resina si compone di due fasi: – la fase di esercizio detta anche di “esaurimento” durante la quale le reazioni vanno da sinistra a destra (si ha cioè la sostituzione degli ioni presenti sui gruppi funzionali con quelli presenti in soluzione) e che si esaurisce con la saturazione di tutti i gruppi funzionali. Questa fase, nell’impianto in oggetto, avviene nei tubi di scambio ionico (5).
– la fase di ricarica detta anche “rigenerazione” nella quale la reazione viene fatta procedere da destra a sinistra ricaricando i gruppi funzionali della resina con gli ioni originari. Nella soluzione proposta, la rigenerazione avviene facendo passare le sfere forate di polietilene, con le resine incorporate, nei tunnels a immersione di liquido rigenerante e di lavaggio (E) costituito da:
– soluzioni basiche, tipicamente sostanze basiche tipo NaOH, NH4OH, nel caso di resine anioniche. In tal caso si ricaricano le resine con gli ioni OH-.
-soluzioni acide, tipicamente a base di acidi forti (HCl, H2SO4) nel caso di resine cationiche. In questo caso si ricaricano le resine con gli ioni H+.
L’elevata concentrazione di ioni H+ e OH–, nei due casi provoca, per la legge di azione di massa, lo spostamento della reazione a sinistra con conseguente ricarica delle resine e rilascio in soluzione degli ioni che nella fase di esaurimento (5) erano stati assorbiti dalle resine. Si ottiene così un eluato generalmente composto da cloruri di vari metalli (nel caso si utilizzi HCl, lo ione H+ ricarica la resina, mentre lo ione Cl– si lega al catione rilasciato dalla resina) o vari sali di sodio nel caso si usi NaOH (lo ione OH– ricarica la resine, mentre allo ione Na+ si lega agli anioni liberati in rigenerazione dalla resina a dare sali di sodio).
ES.: Ca++ + 2HCl → CaCl2 + 2 H+; SO4— + 2NaOH → Na2SO4 + 2OH.
Le resine a scambio ionico per il fatto che scambiano idrogenioni (cationiche) e idrossilioni (anioniche) vengono più propriamente definite resine cationiche in ciclo acido (R-H) e resine anioniche in ciclo basico (R-OH), in ragione delle caratteristiche degli ioni rilasciati i quali rendono le acque acide o basiche.
Di seguito sono riportate alcune reazioni di scambio ionico per resine sintetiche:
Resine cationiche forti:
R-SO3H + Na+↔ R-SO3Na + H+; 2R- SO3Na + Ca2+ ↔ (R-SO3)2Ca + 2Na+.
Resine cationiche deboli:
R-COOH + Na+ ↔ R-COONa + H+; 2R-COONa + Ca2+ ↔ (RCOO)2Ca + 2Na+
Resine anioniche forti:
RR’3NOH + Cl–↔ RR’NCl + OH–.
Resine anioniche deboli:
RNH3OH + Cl– ↔ RNH3Cl + OH–; 2RNH3Cl + SO42-↔ (RNH3)2SO4 + 2Cl–.
ESEMPIO DI SCAMBIO E RIGENERAZIONE.
Rimozione degli ioni Sodio (Na+) e Calcio (Ca2+) dall’acqua utilizzando una resina cationica forte. Reazione: R- H+ +Na+→ R -Na+ +H+; 2R– Na+ + Ca2+ → R2–Ca2+ + 2Na+
Rigenerazione:
la rigenerazione viene effettuata con acido cloridrico (HCl) e cloruro di sodio (NaCl)
R–Na+ + HCl → R–H+ + NaCl; R2–Ca2+ + 2NaCl → 2R–Na+ + CaCl2.
La selettività di una resina, cioè il fatto che scambi uno ione presente in soluzione con quelli nei siti attivi, piuttosto che un altro, dipende dalla natura e dalla valenza dello ione, dal tipo di resina, dalla sua saturazione, nonché dalla concentrazione di uno specifico ione in soluzione. Generalmente tale selettività resta valida in un ristretto campo di pH. Tipicamente la scala di selettività o se vogliamo di affinità di scambio delle resine cationiche risulta essere:
Li+ < H+ < Na+ < NH4+ < K + < Rb+ Ag+ Mg2+ < Zn2+ < Co2+ < Cu2+ < Ca2+ < Sr2+ < Ba2+ ; mentre per le resine anioniche risulta: OH– <<< F–< HCO– < Cl– < Br– < NO3– < ClO4–
Negli attuali sistemi di scambio ionico la fase di esercizio prevede, generalmente, il passaggio dell’acqua in un serbatoio riempito di resina e una portata di acqua che deve essere tenuta entro certi limiti per garantire adeguati tempi di scambio. I dati caratteristici sono molto variabili in funzione della quantità di sali e del ph: portata di esercizio compresa fra 5 e 50 litri/h/litro resina. E’ molto difficile gestire e controllare un processo completo, soprattutto, se è necessario dissalare grandi portate di acqua. Anche la fase rigenerativa, attualmente, non è facile da gestire. Essa si suddivide in tre sottofasi.
a) Lavaggio in controcorrente (backwash): acqua in flusso ascensionale, velocità del flusso pari a 10-15 m/h, espansione del letto di resina del 50-70 %. Tale lavaggio serve ad eliminare eventuali percorsi preferenziali formatisi durante la fase di scambio e a rimuovere le impurità che si fossero eventualmente formate nel letto durante la fase di scambio. La durata di questa fase, negli impianti esistenti, è di circa 15 minuti.
b) La rigenerazione può essere acida o basica a seconda che riguardi una resina a scambio cationico o anionico rispettivamente. Le soluzioni utilizzate sono soluzioni diluite la cui percentuale di acido o base disciolta dipende dalla forza (grado di dissociazione) dello stesso. Ad esempio per ricaricare una resina cationica si possono utilizzare soluzioni acide quali:
5 – 10 % di HCl ad una portata di 3 -4 l/h/l resina
1 – 3 % di H2SO4 ad una portata di 10 – 15 l/h/l resina
c) Lavaggio finale che viene effettuato con acqua demineralizzata in down flow in due fasi:
una prima fase alla portata della fase rigenerativa per lavare l’acido residuo;
una seconda fase alle condizioni di esercizio per un volume complessivo d’acqua pari a 6 – 9 volumi di resina.
La nuova impiantistica elettromeccanica e idraulica dello scambio ionico.
La lunga introduzione, sopra riportata, che ha riassunto lo stato dell’arte dei processi chimici e fisici che governano il complesso sistema dello scambio ionico è fondamentale per comprendere le ragioni per le quali è nata questa invenzione. Infatti, i cicli di lavoro degli attuali impianti che utilizzano lo scambio ionico sono il punto di partenza per la progettazione di questi nuovi impianti, che non devono stravolgere i principi basilari, ma li devono soltanto rendere più economici, soprattutto, abbinando la produzione di energia idroelettrica, a basso costo, che venduta ai gestori, di fatto, abbassa il costo della desalinizzazione. Infatti, l’energia idroelettrica prodotta senza il classico salto idraulico, è molto più economica dell’attuale energia idroelettrica, non richiedendo la costruzione di dighe e bacini. Basta soltanto lo sfruttamento dell’energia di posizione delle acque poste nella posizione alta di un sistema idrico mantenuto sempre pieno per sfruttare regimi idraulici vantaggiosi ai fini energetici. Pertanto, gli impianti, con scambio ionico, abbinati alla produzione di energia, oltre alla desalinizzazione e demineralizzazione, possono avere anche altre applicazioni depurative, visto che anche le acque dolci, in moltissimi casi, anche quando sono estratte dal sottosuolo, devono essere private di sostanze indesiderate a causa delle numerose infiltrazioni dovute ai prodotti chimici usati in agricoltura, nelle industrie, nelle attività urbane, infiltrazioni di solventi e metalli radioattivi liberati nei pressi di trivellazioni con il sistema della fratturazione acqua solventi e materiali inerti ad alta pressione. Certamente, anche l’ultra filtrazione può essere abbinata alla produzione dell’energia idroelettrica, riducendo i costi di esercizio, ma gran parte dell’energia sarebbe consumata nello stesso impianto, mentre il costo per la sostituzione delle membrane usurate non sarebbe risolto. Inoltre, è necessario precisare che allo stato dell’arte, non si dissala l’acqua di mare ma soltanto le acque salmastre perché dissalare le acque del mare costerebbe circa 3,5 volte i costi attuali, che già non sono sostenibili per impieghi su larga scala. Infatti, nel processo per osmosi inversa, l’acqua da dissalare è messa in comunicazione con acqua dolce attraverso una membrana permeabile al solo solvente; applicando dal lato della soluzione salina una pressione superiore a quella che si genera per osmosi, s’inverte il normale senso di diffusione e il solvente tende ad abbandonare la soluzione con più alto tenore di sali. Il processo non viene ancora impiegato per la dissalazione di acqua di mare, in quanto, essendo la pressione osmotica fra acqua di mare (salinità media: 35 g/l) e acqua distillata pari a circa 22 bar, la corrispondente pressione richiesta per ottenere un apprezzabile flusso di solvente attraverso la membrana può anche superare 100 bar. Il processo trova, invece, applicazione per la dissalazione di acqua salmastra con salinità inferiore a 10 g/l. Nella stessa proporzione si incrementano anche i costi energetici dei processi evaporativi, mentre con lo scambio ionico proposto aumentano soltanto i costi degli additivi chimici e della quantità di resine necessarie.
Prima di iniziare la descrizione del processo è opportuno riportare le legende delle figure che illustrano l’impianto.
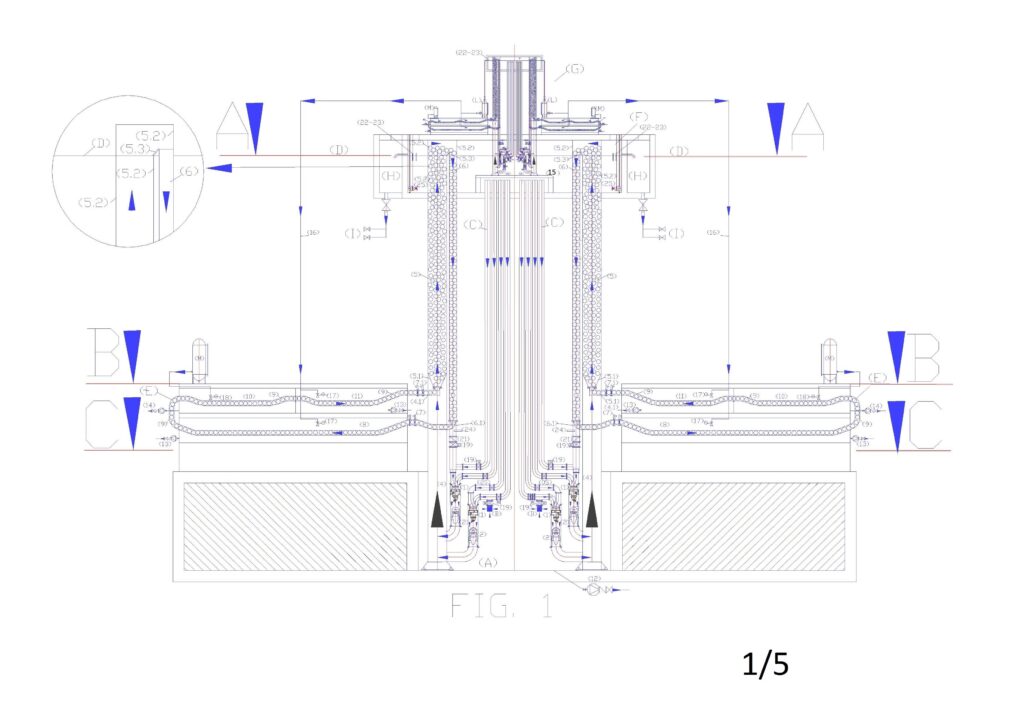
Legenda alfabetica: (A) bacino di arrivo acqua salata = arrival basin of salted water; (B) filtro di aspirazione acqua salata con valvola di ritegno incorporata = salt water inlet filter with built-in check valve; (C) tubo di riciclo acqua e pressurizzazione dinamica o cinetica della elettropompa = Water recirculation tube and dynamic or kinetic pressurization of the electric pump; (D) livello nominale bacino superiore = Nominal upper basin level; (E) circuito di lavaggio e rigenerazione resine di scambio ionico = washing and regeneration circuit of ion exchange resins; (F) serbatoio superiore di miscelazione e sfioro acque desalinizzate = upper reservoir mixing and overflow desalinated water; (G) Mini impianto di produzione acqua deionizzata = Mini implant of deionized water production; (H) serbatoio di accumulo acque desalinizzate = desalinated water storage basin; (I) rete di distribuzione acqua desalinizzata = desalinated water distribution network; (L) serbatoio di accumulo acqua demineralizzata = demineralized water accumulation tank; (M) serbatoio con liquido rigenerante = regenerating liquid tank.
Legenda numerica: (1) pompa capovolta con doppia alimentazione sul lato aspirante = overturned dual supply pump on the suction side; (2) turbina sommersa con alternatore incorporato = submerged turbine with incorporated alternator; (3) livello nominale bacino acqua da dissalare = nominal level of the water basin to desalinate; (4) tubo di alimentazione acqua da dissalare = pipe for supplying water to desalinate; (4.1) pezzo speciale per introduzione sfere con resine nel tubo di scambio ionico (forato nella parte inferiore) = special piece for introduction spheres with resins in the ion-exchange tube (drilled in the lower part); (5) tubo di scambio ionico = tube of ion exchange; (5.1) tronco conico forato incorporato nel tubo 5 = perforated truncated cone embedded in the tube 5; (5.2) pezzo speciale per fuori uscita sfere dal tubo 5 (forato su tutta la superficie esterna e collegato al tubo 6 per mezzo dello scivolo 5.3) = special piece to eject spheres from the tube 5 (perforated on the entire outer surface and connected to the tube 6 by means of the slide 5.3); (5.3) scivolo in lamiera per la guida delle sfere nel tubo 6 ) = metal sheet slide for the guidance of the spheres in the tube 6; (6) tubo di discesa sfere per lo svuotamento dell’acqua = tube of descent spheres for the emptying; (6.1) pezzo speciale per la deviazione delle sfere dal circuito di scambio ionico al circuito di rigenerazione (forato nella parte inferiore per lo scolo dell’acqua) = special piece for the deviation of the spheres from the ion exchange circuit to the regeneration circuit (drilled at the bottom for water drainage); (7) valvole a ghigliottina automatizzate per arresto circolazione sfere (sono sempre aperte quando la sonda di minimo livello indica che il tubo 6 è vuoto di acqua = automated guillotine valves for stopping movement spheres (are always open when the minimum level probe indicates that the tube 6 is empty of water; (7.1) valvole a ghigliottina automatizzate per arresto circolazione sfere (si aprono una per volta) = automated guillotine valves for stopping movement spheres (open one at a time); (8) primo tunnel per lavaggio a immersione delle resine = first tunnel for immersion wash of the resins; (9) percorso guidato delle sfere nei tunnel a immersione con un telaio aperto di tondini di acciaio inox con salite e discese dotate di scivoli per la raccolta del liquido di svuotamento delle sfere = guided route of the spheres in the immersion tunnel with an open frame of stainless steel rods by ascents and descents with slides for the collection of the of the spheres emptying liquid; (10) tunnel per rigenerazione a immersione delle resine = tunnels for regeneration of the resins in immersion; (11) secondo tunnel di lavaggio a immersione delle resine = second washing immersion tunnel of the resins; (12) elettropompa di estrazione fanghi dal serbatoio di arrivo = pump suction sludge from arrival reservoir; (13) elettropompa di estrazione fanghi di lavaggio resine = electric pump suction of resin washing sludge; (14) elettropompa di estrazione fanghi di rigenerazione resine = electric pump suction of resins regeneration sludge; (15) Telaio di sostegno impianto di demineralizzazione = Support frame demineralisation plant; (16) tubo di alimentazione acqua demineralizzata = supply pipe demineralized water; (17) valvola a galleggiante per alimentazione acqua demineralizzata = float valve for feeding demineralized water; (18) valvola a galleggiante per alimentazione liquido rigenerante = float valve for regenerating liquid supply; (19) valvola motorizzata di intercettazione = motorized shut-off valve; (20) valvola manuale di intercettazione = Manual shut-off valve; (21) valvola di ritegno = check valve; (22) sonda di controllo salinità = salinity control probe; (23) sonda di controllo PH = PH control probe. (24) sonda di controllo minimo livello acqua del tubo di svuotamento sfere = minimum water level control probe of spheres emptying tube; (25) agitatore sommerso = submerged agitator.
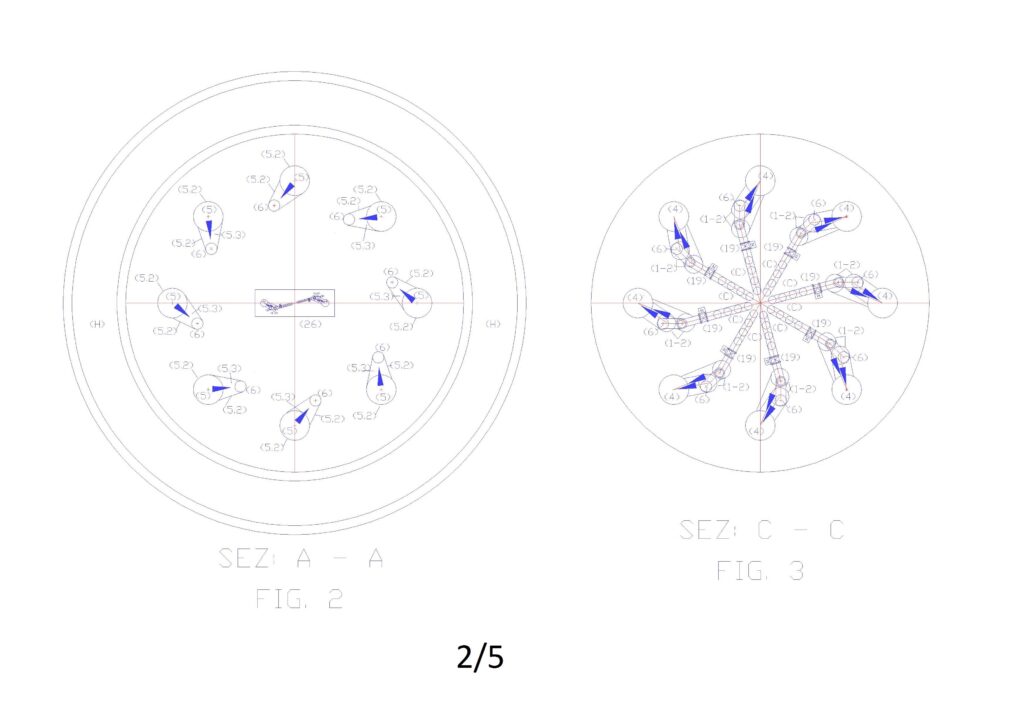
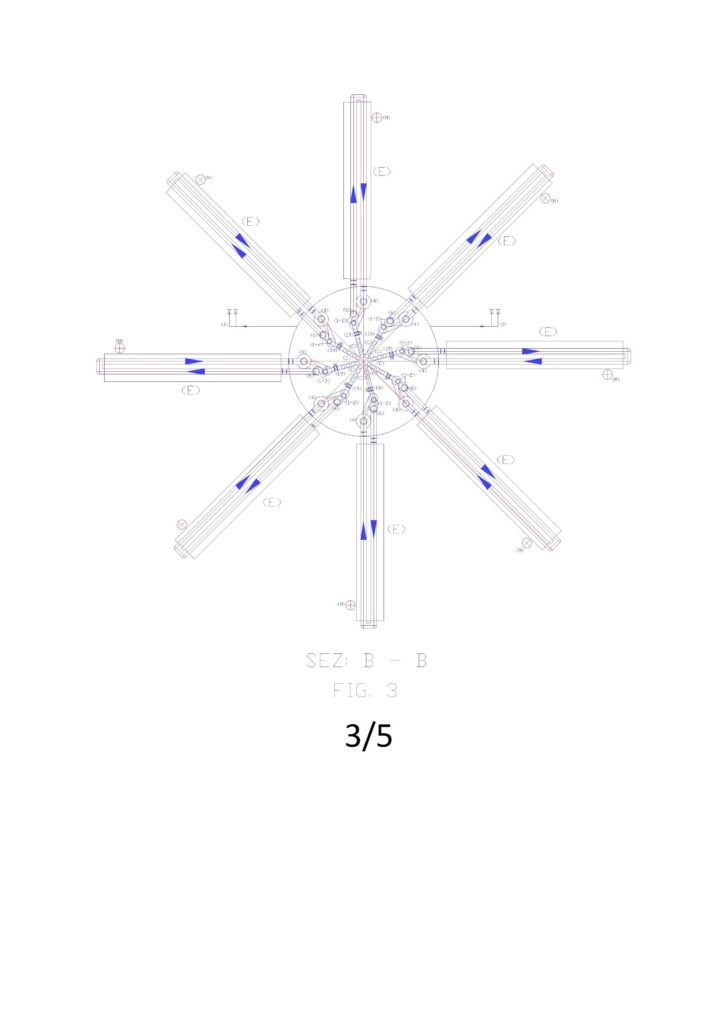
La figura “1” riporta lo schema generale dell’impianto in verticale, dove si possono notate in sezione gli elementi riportati nelle legende, mentre le figure 2, 3, 4, riportano le sezioni ai piani altimetrici A, B, C.
Luigi Antonio Pezone